2021年4月29日,深圳市先健心康医疗电子有限公司自主研发的国家创新产品“8301临时起搏器”获得国家药品监督管理局(NMPA)注册批准。该创新产品是国产首个具有完全自主知识产权的临时起搏器,获批当日即获得市场巨大关注,人民网等众多权威媒体跟进报道,更以极高热度冲上当日微博热搜榜前列,阅读量高达9000余万。

该产品使用两节5号电池供电,并通过自带的患者电缆和起搏电极导线连接,共同构成一个起搏系统。对比同类进口产品,8301临时起搏器针对我国临床的实际需求,采用了独特的分析、起搏二合一设计。它既可用于心动过缓患者的临时起搏治疗,也可作为一台起搏系统分析仪使用,对起搏系统的阻抗和感知幅值进行实时连续测量和显示。此外,该产品独创性地采用了图形点阵液晶屏,可以实时显示腔内心电图,并提供起搏和感知标记,方便医生观察术中损伤电流。
临时起搏器在抢救严重心动过缓患者,提供临时起搏保护上有着药物无法替代的重要价值,是临床必须的急救,治疗和保护设备。临时起搏器也是我国二级及以上医院评定必须具备的临床技能所需设备。起搏系统分析仪是永久起搏器植入手术中必须使用的设备,用来测量起搏系统的电学参数并判断其是否达到临床要求。
近几年,随着心脏起搏疗法进一步普及和大量的医院/病房新建和改扩建,心脏中心、胸痛中心和县医院能力建设等,越来越多的医院/医生开始开展临时起搏的临床急救和永久起搏器植入手术,临时起搏器和起搏系统分析仪的需求在逐步放大。
本次批准的产品由海外归国的曾乐朋博士的研发团队历时两年研发成功。其主要功能达到或超过进口同类产品的水平。曾乐朋博士曾担任美敦力公司(US:MDT)首席科学家和先健科技(HK:1302)首席医学官。他领导的研发团队具有丰富的心脏节律管理等三类医疗器械研发经验,早先帮助先健科技公司完成了中国首个植入式心脏起搏系统-芯彤起搏器的国产化工作。8301临时起搏器根据临床使用习惯进行了全新设计,曾获得德国红点设计奖,并于2019年和2020年分别获得了美国FDA认证和欧盟CE认证,是国内目前唯一获得国外权威认证的临时起搏器。
临床试验
8301临时起搏器的上市前临床研究邀请了我国知名心血管疾病专家广州中山大学附属第一医院董吁钢教授作为主要研究者,在中山大学附属第一医院、中山大学孙逸仙纪念医院和南方医科大学南方医院总计入组了104名患者。临床试验结果验证了该产品一方面在临时起搏时VVI起搏模式工作良好,起搏与感知功能有效安全,另一方面在分析功能上与进口同类产品的测试结果高度一致,完全符合临床要求。
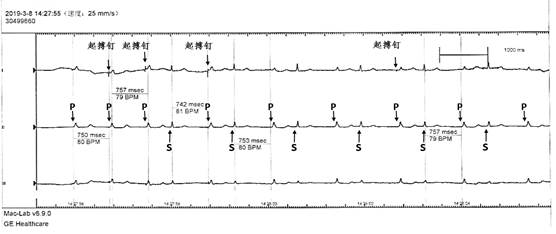
如上图所示,8301临时起搏器在VVI工作模式下工作正常,起搏节拍和感知的自身节拍交替出现,且出现的条件符合VVI起搏准则。部分起搏心律可在I导联上对应的时间位置观察到起搏钉。P代表起搏节拍,S代表感知节拍。
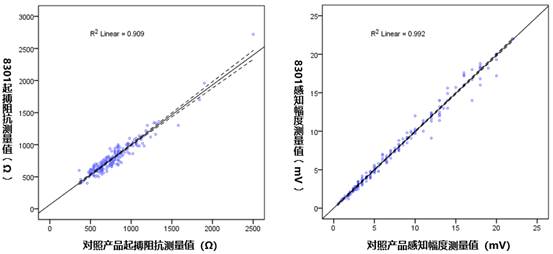
如上图所示,8301临时起搏器对起搏阻抗和感知幅度的测量值和进口同类产品的测试结果高度一致。
公司介绍
深圳市先健心康医疗电子有限公司成立于2017年11月。公司以开发临时起搏器及其配套导线等系列产品为契机,在心脏节律管理和神经调控领域构建完整的有源医疗器械技术平台,填补国内产业空白,逐步实现相关产品设备的产业化。企业预期成长为中国心脏节律管理和神经调控领域完善解决方案的供应商,能够为国内医疗机构和广大患者提供从监测、诊断、治疗到术后随访的全套解决方案。